肺结节是不是癌? 手术还是继续随访? 会不会癌变? …… 这些问题 已经成为大多肺结节患者的心头之痛 为此 广州医科大学附属第一医院 国家呼吸医学中心 何建行教授团队 经过多年探索研发出一项“黑科技” 可辅助精准判断 不确定肺结节的良恶性 准确率达91% 该研究成果在国际顶级学术期刊The Lancet Digital Health(影响因子30.8)上正式发表,这是该团队继2021年在Journal of Clinical Investigation发表自主研发的全球首个基于cfDNA甲基化高通量测序液体活检技术的肺结节诊断模型PulmoSeek的建模与验证数据之后,再一次对该模型进行多模态升级。研究的主要共同完成人为何建行、曾庆思、范建兵、梁文华。 迄今为止,在已公开发表的基于cfDNA甲基化技术进行肺结节良恶性鉴别诊断的研究中,本研究纳入样本量最大、入选中心最多,是国际首个联合cfDNA甲基化标志物、临床信息和影像学特征用于机器学习建模并开发的多模态诊断模型(PulmoSeek Plus模型)用于肺结节良恶性鉴别,针对不同大小、不同类型肺结节亚组均有优异的诊断性能和潜在临床应用价值。 尤其是可以协助5-10mm不确定结节分流管理,可减少85%的良性结节不必要的侵入性检查/手术、避免72%的恶性结节被延误治疗。 1+1>2:CT影像+血浆甲基化联合提升诊断准确性 肺癌的早期诊断仍然是一个世界难题。临床亟需一种稳定、灵敏、无创的能“精准判定”肺结节良恶性的工具。 研究团队前期已建立了一种基于血液的cfDNA甲基化模型(PulmoSeek,包含100个甲基化位点)用于肺结节的良恶性诊断。这一工具已得到全国多中心临床研究的验证。 理论上,影像特征对ctDNA非脱落病灶有更好的敏感性,而cfDNA生物标志物则更为特异,两者有一定互补性。 因此,团队在本研究中整合了cfDNA甲基化、临床特征和CT影像特征,运用机器学习算法开发了一个组合模型PulmoSeek Plus,该模型的综合诊断性能优于单独的甲基化模型PulmoSeek和影像学模型CIBM。 研究分为三个阶段,共计入组1076例肺癌和304例非肺癌入组者的血液样本。 为了证实cfDNA甲基化和CT影像特征有1+1>2的效果,本研究开发了新的肺结节良恶性分类模型PulmoSeek Plus:PulmoSeek模型+CIBM模型。 研究发现,该模型各期肺癌的敏感性≥95%,整体敏感性为0.98,对早期肺癌(0/I期)敏感性为0.98;对不同大小恶性结节的敏感性≥98%,整体敏感性为0.98,对不确定结节(5-10mm)敏感性为0.99。 值得注意的是,当发病率为10%时,该模型校正后的阴性预测值(NPV)高达1.0。 PulmoSeek Plus模型在早期肺癌和小结节中的检测灵敏度
近日,由何建行教授团队牵头,联合基准医疗及全国24家中心共同合作开发,运用外周血cfDNA甲基化标志物、临床信息和影像学特征构建了肺结节良恶性分类模型,用于肺癌的早期诊断。
 模型构建(CIBM、IBMI和PulmoSeek Plus)
模型构建(CIBM、IBMI和PulmoSeek Plus)
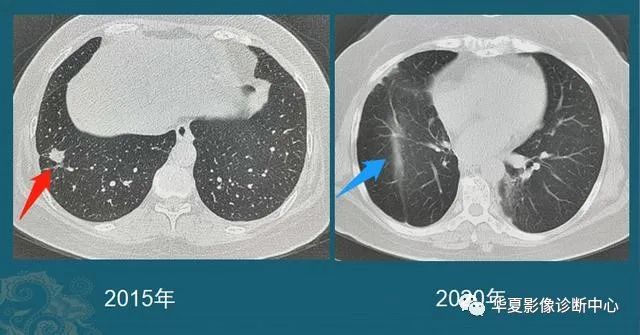
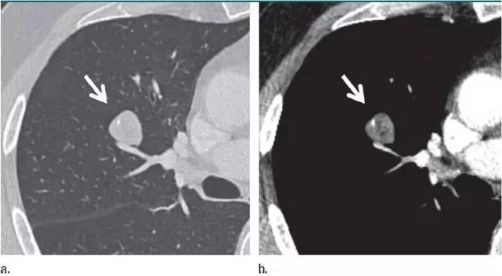
1cm以下的微小肺结节也能鉴别
为了兼顾“排阴(rule-out)”和“确阳(rule-in)”的临床需求,本研究同时应用PulmoSeek Plus的两个cut-off(高灵敏度/低特异性 vs. 高特异性/低灵敏度)将不确定结节(IPN, 5-10mm)重新分类成低风险、中风险和高风险。
在541例合并数据集里,利用PulmoSeek Plus模型“三分法”重分类可减少89%的良性结节不必要的侵入性检查/手术、避免73%的恶性结节被延误治疗。
由于不确定结节在临床实践中非常难判定良恶,本研究将5-10mm的小结节定义为不确定结节,利用PulmoSeek Plus模型“三分法”重分类可减少85%的良性结节不必要的侵入性检查/手术、避免72%的恶性结节被延误治疗。
结果表明,PulmoSeek Plus模型在不同的临床场景有较优异的诊断性能,即使对不确定结节(IPN, 5-10mm)也保持优异的综合性能。

PulmoSeek Plus模型“三分法”定义肺结节风险
国际认可:柳叶刀子刊同期点赞
本研究通过机器学习创新地整合了cfDNA 甲基化生物标志物、临床和影像特征,建立了多模态联合诊断模型 PulmoSeek Plus,可显著提高早期恶性肺结节的检出率,避免良性肺结节的过度诊疗,有利于辅助临床诊疗决策,助力于肺癌的早发现、早治疗。
与此同时,The Lancet Digital Health同期发表了评论“Classification of pulmonary nodules in the era of precision medicine”,对本研究给予了积极评价,认为:“这项研究为在精准医学时代识别肺结节的良恶性提供了一个有价值的工具,也为该领域的未来研究提供了新的见解。将多组学数据与机器学习算法相结合是未来提高诊断效率的一种有前途且有效的方法。”
主要共同完成人
何建行
广州医科大学附属第一医院
胸外科,器官移植科,肿瘤科
教授、主任医师、博士生导师
国家呼吸医学中心主任
广州呼吸健康研究院院长
美国外科学院、英国皇家外科学院Fellow
美国胸心外科学会、欧洲心胸外科协会Member
专业方向:
全球首创无管自主呼吸的气道手术,针镜手术,异位心肺联合移植等移植新技术:亚洲首例同种异体气管移植术;国内首例全胸腔镜肺癌根治术等。创新及发展了胸外科 “无管”微创技术系统,在2021年被列入了哈佛大学教程。提升了肺癌无创早诊技术,制定了个体化术后治疗新策略,以第一/通讯作者在NEJM、Lancet、cell. Nat Med等发表SCl论文400余篇,获评2020年爱思唯尔(呼吸与胸外科)“十大中国高被引学者之一〞及2021全球学者库(胸心外科)学术影响力排名“全球第五〞;主编英文专著8部;获24项国家发明专利;国际专利1项;1项研究写入WHO新冠防治指南、1项研究列入美国临床肿癌指南(NCCN)1项研究肺癌预后模型被美国国家癌症研究所Knight中心唯一推荐、1项研究被美国列入商业保险项目、4项研究被列入WHO全球慢阻肺指南依据。牵头制定首个无管微创手术 (TubelessVATS)国际共识、肺癌新辅助免疫治疗国际共识。获2018年国家科技进步二等奖(排名第一):中华医学科技一等奖(排名第一)等4项省部奖。获2020年国家创新争先奖牌、广东省科技特等奖及2021年国家科技进步一等奖(创新团队)。创办了JTD和ATM两本SCI杂志。
曾庆思
广州医科大学附属第一医院
医学影像科教授
主任医师,硕士生导师
中华医学会放射学分会心胸专业委员会资深委员、中国医师协会呼吸医师分会呼吸放射工作委员会委员、广东省胸部疾病学会影像专业委员会主任委员、广东省粤港澳合作促进会理事会理事、广东省胸部疾病学会理事、广东省医学会放射学分会委员兼心胸学组组长、广东省和广州市新冠肺炎专家组影像专家等。
专业方向:
擅长胸部疑难病、少见病的影像诊断。胸部疾病影像诊断水平在国内享有较高声誉。在国内外发表医学专业论文一百多篇,主编、参编医学专著多本;主持及参与包括国家卫计委行业专项基金项目子项目、国家自然科学基金面上项目和省科技计划项目等多项科研项目,曾获广东省科技二等奖及广州市科技进步奖二等奖。获得广东省抗击非典功臣称号。
出诊时间(大坦沙院区):
周二上午;周三下午;周四下午
梁文华
广州医科大学附属第一医院
教授、副主任医师、博士生导师
胸部肿瘤综合诊疗病区负责人
国家优秀青年基金获得者(肿瘤学)
青年珠江学者
人民网“国之名医·青年新锐”
广州呼吸健康研究院院长助理
国家呼吸医学中心办公室主任
广东省胸部疾病学会免疫治疗分会主任委员、广东省医学会精准医学与分子诊断分会副主任委员、国家呼吸疾病重点实验室肺癌学组副组长、国际肺癌研究协会(IASLC)成员、阿里达摩院青橙奖首位医学获得者、Transl Lung Cancer Res杂志副主编等。
专业方向:
擅长肺癌、肺结节的综合诊治:肺癌新疗法(靶向及免疫治疗等)、精细化管理以及早诊早治(小结节鉴别及术后长期随访)等。主攻肺癌的综合诊疗及临床转化研究,曾于国际顶尖期刊NEJM,J Clin Oncol,Lancet Oncol,BMJ等发表200余项学术成果,总被引超过2万次,H指数35。承担国家级及省市级科研项目5项,主持国内多个多中心临床研究。2020年国家科技进步一等奖创新团队、2018年中国科技进步二等奖主要完成人之一。作为主编/副主编著有《肺癌早期检测及诊断》专刊、《肺癌》、《Lung Cancer》等。