对于人类表皮生长因子受体HER2阳性且激素受体阳性晚期乳腺癌绝经患者,HER2靶向治疗可显著提高内分泌治疗的临床获益。HER2双靶向药物与HER2单靶向药物相比,临床获益也可显著提高。不过,对于术前新辅助或术后辅助或转移后曲妥珠单抗+化疗失败后不再考虑或无法耐受化疗的HER2阳性且激素受体阳性晚期乳腺癌绝经患者,HER2双靶向药物+内分泌治疗的有效性和安全性尚不明确。
2020年8月21日,美国临床肿瘤学会《临床肿瘤学杂志》在线发表ALTERNATIVE研究报告更新,对Apatinib/ target=_blank class=infotextkey>LApatinib/ target=_blank class=infotextkey>拉帕替尼+曲妥珠单抗+芳香酶抑制剂、曲妥珠单抗+芳香酶抑制剂、Lapatinib/ target=_blank class=infotextkey>拉帕替尼+芳香酶抑制剂三种方案一线或二线治疗HER2阳性且激素受体阳性晚期乳腺癌曲妥珠单抗+化疗失败患者的有效性和安全性进行了比较。
01 研究设计:
ALTERNATIVE研究是一项国际多中心非盲随机平行对照三期临床研究,2011年5月5日~2016年3月11日从29个国家地区112家医院入组曲妥珠单抗+化疗失败后不再考虑化疗的HER2阳性且激素受体阳性晚期乳腺癌绝经患者355例,按1∶1∶1的比例随机分为三组:
拉帕替尼(LAP)+曲妥珠单抗(TRAS)+芳香酶抑制剂(AI):120例;
曲妥珠单抗(TRAS)+芳香酶抑制剂(AI):117例;
拉帕替尼(LAP)+芳香酶抑制剂(AI):118例;
芳香酶抑制剂为研究者自行选择的来曲唑、阿那曲唑、依西美坦三者之一。
主要终点为研究者评定的无进展生存(拉帕替尼+曲妥珠单抗+芳香酶抑制剂、曲妥珠单抗+芳香酶抑制剂两组相比)。次要终点为无进展生存(其他组相比)、总生存、客观缓解比例、临床获益比例、安全性。
02 研究结果:
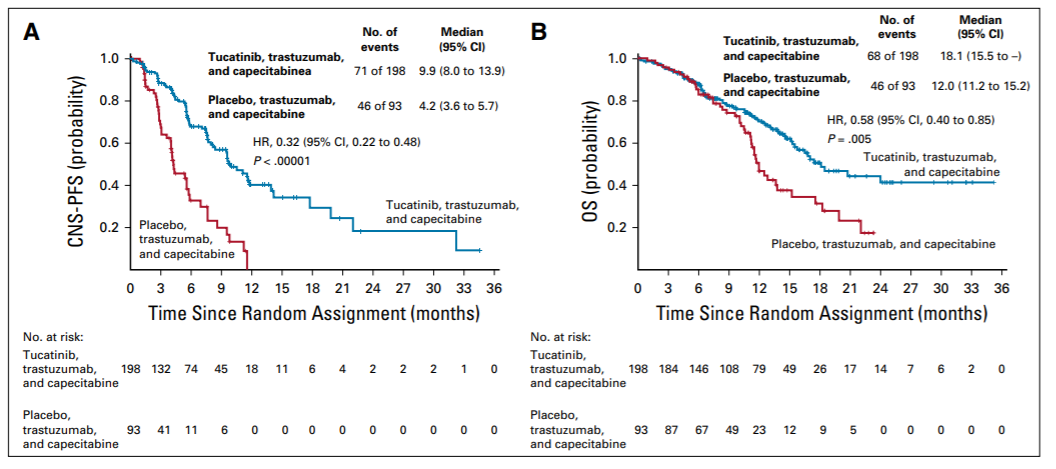
(1)PFS:拉帕替尼+曲妥珠单抗+芳香酶抑制剂、曲妥珠单抗+芳香酶抑制剂、拉帕替尼+芳香酶抑制剂三组中位PFS分别为11个月、5.6个月、8.3个月。
拉帕替尼+曲妥珠单抗+芳香酶抑制剂、曲妥珠单抗+芳香酶抑制剂两组相比,中位无进展生存将近2倍(11个月比5.6个月),进展或死亡风险显著减少38%(风险比:0.62,95%置信区间:0.45~0.88,P=0.0063)。
拉帕替尼+芳香酶抑制剂、曲妥珠单抗+芳香酶抑制剂相比,中位无进展生存将近1.5倍(8.3比5.6个月),进展或死亡风险减少15%(风险比:0.85,95%置信区间:0.62~1.17,P=0.3159)。

(2)ORR和OS:拉帕替尼+曲妥珠单抗+芳香酶抑制剂、曲妥珠单抗+芳香酶抑制剂、拉帕替尼+芳香酶抑制剂三组ORR分别为31.7%、13.7%和18.6%。
拉帕替尼+曲妥珠单抗+芳香酶抑制剂、曲妥珠单抗+芳香酶抑制剂、拉帕替尼+芳香酶抑制剂三组OS分别为46个月、40个月和45.1个月。

(3)安全性:拉帕替尼+曲妥珠单抗+芳香酶抑制剂、曲妥珠单抗+芳香酶抑制剂、拉帕替尼+芳香酶抑制剂相比,发生比例≥15%的不良事件:
腹泻:69%、9%、51%;
皮疹:36%、2%、28%;
恶心:22%、9%、22%;
甲沟炎:30%、0%、15%;
大多为1或2级,三组三级以上不良反应率分别为34%、22%和32%。

HER2阳性乳腺癌约占乳腺癌全部类型的20%至25%,并与不良预后和生存有关。约50%的HER2阳性乳腺癌是激素受体(HR)阳性。HER2阳性/ HR阳性的BC约占所有BC的10%。HER2阳性转移性乳腺癌(MBC)的患者通常化疗,HER2靶向药物曲妥珠单抗,拉帕替尼,帕妥珠单抗和曲妥珠单抗ADC(T-DM1)等药物在HER2阳性MBC中具有显着改善的治疗效果。临床前研究已证明双抗TRA2加PTZ加化疗一线治疗HER2阳性乳腺癌可提高疗效。但并非所有HER2阳性/ HR阳性MBC的患者都耐受化疗,同时靶向HER2和ER可能对HER2阳性/ HR阳性MBC具有显著的临床效果。
以往研究证明,在HER2阳性/ HR阳性MBC一线治疗中,与单独采用内分泌疗法(ET)相比,在一线治疗中联合HER2药物显示出很好的临床获益。与单独使用每种ET相比,TRAS联合阿那曲唑(ANA)或LAP联合来曲唑(LET)可以显着降低进展风险。
本研究进一步证明,对于HER2阳性且激素受体阳性晚期乳腺癌曲妥珠单抗+化疗失败后不再考虑或无法耐受化疗的绝经患者,拉帕替尼+曲妥珠单抗双靶向药物阻断+芳香酶抑制剂与曲妥珠单抗+芳香酶抑制剂相比,无进展生存获益显著较大。三级以上不良反应较低,安全性良好。该联合方案为此类患者提供了有效而安全的化疗替代方案。
参考文献
Johnston SRD, Hegg R, Im SA, et al. Phase III, Randomized Study of Dual Human Epidermal Growth Factor Receptor 2 (HER2) Blockade With Lapatinib Plus Trastuzumab in Combination With an Aromatase Inhibitor in Postmenopausal Women With HER2-Positive, Hormone Receptor-Positive Metastatic Breast Cancer: Updated Results of ALTERNATIVE [published online ahead of print, 2020 Aug 21]. J Clin Oncol. 2020;JCO2001894. doi:10.1200/JCO.20.01894