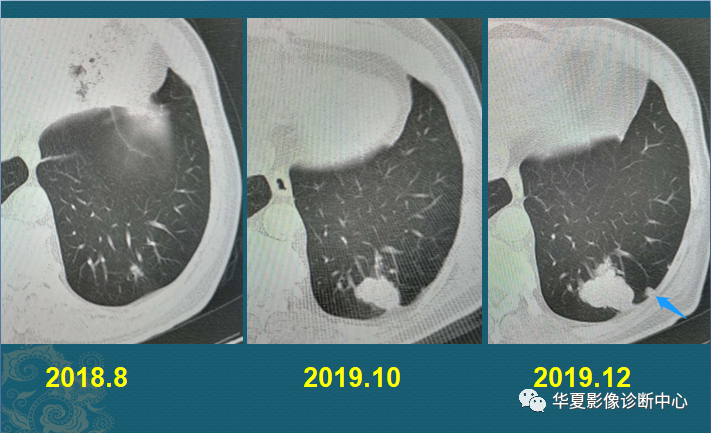
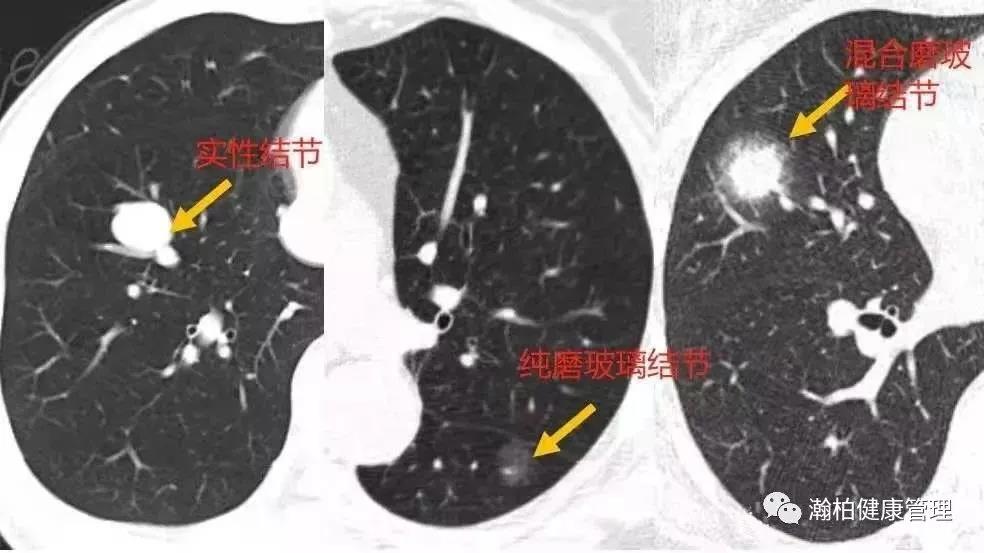
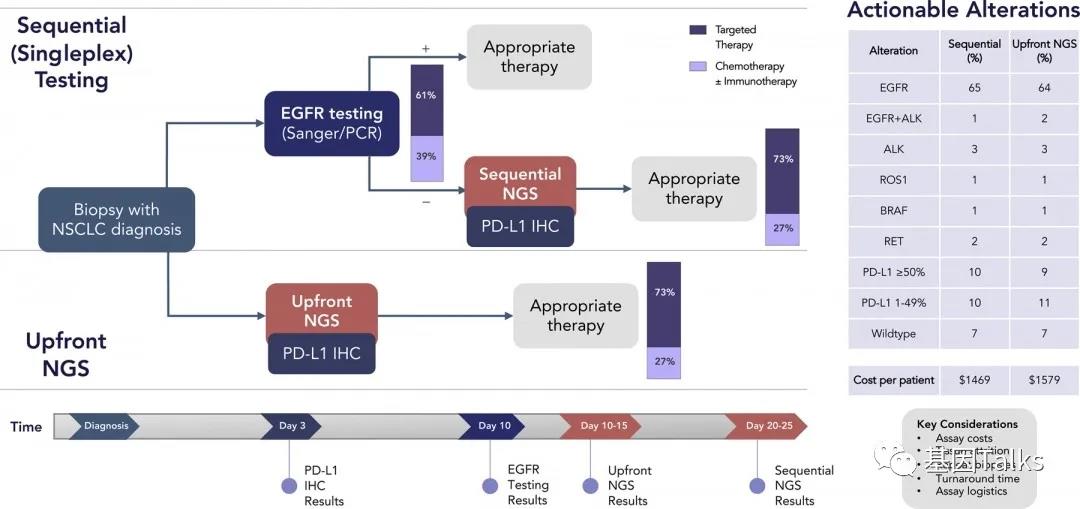
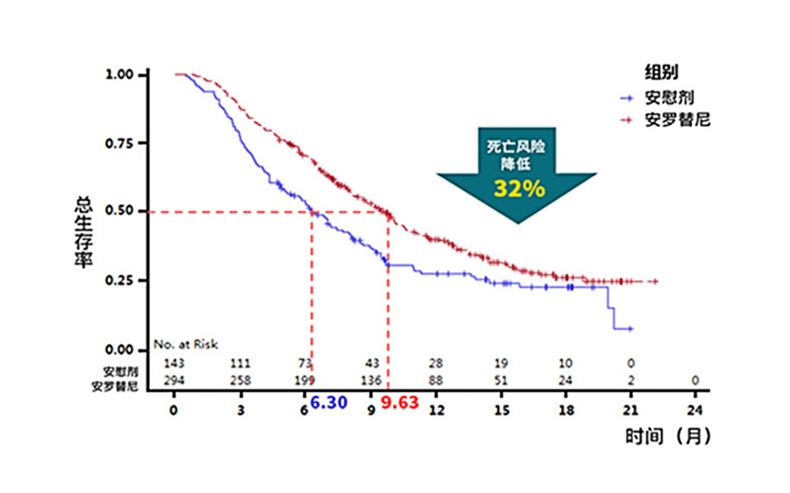
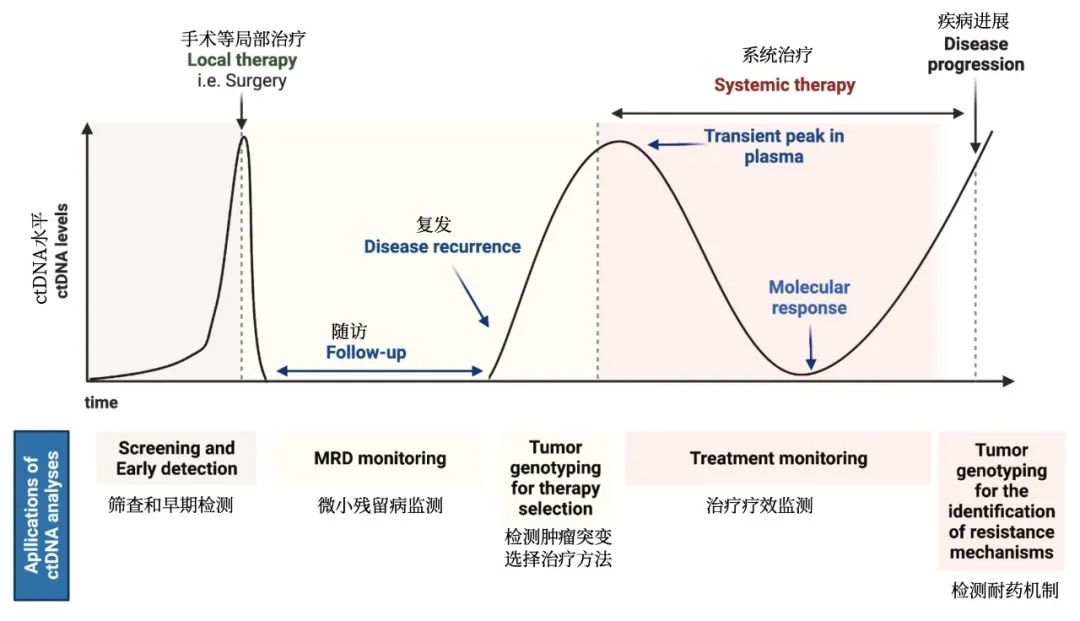
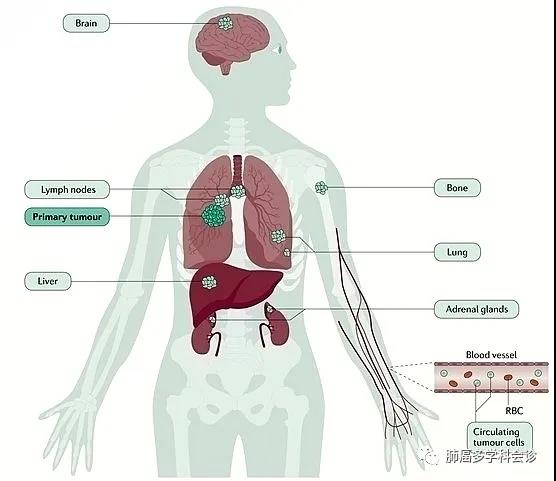
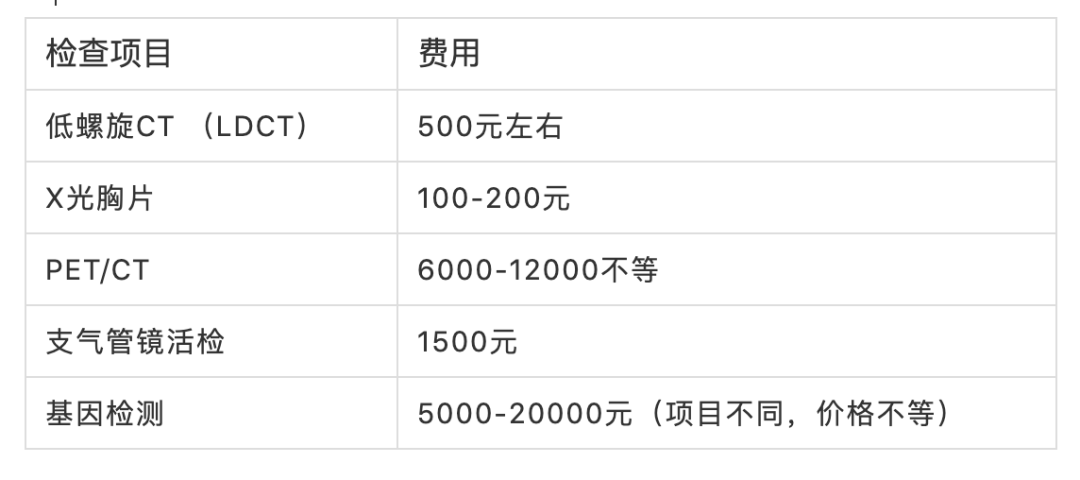
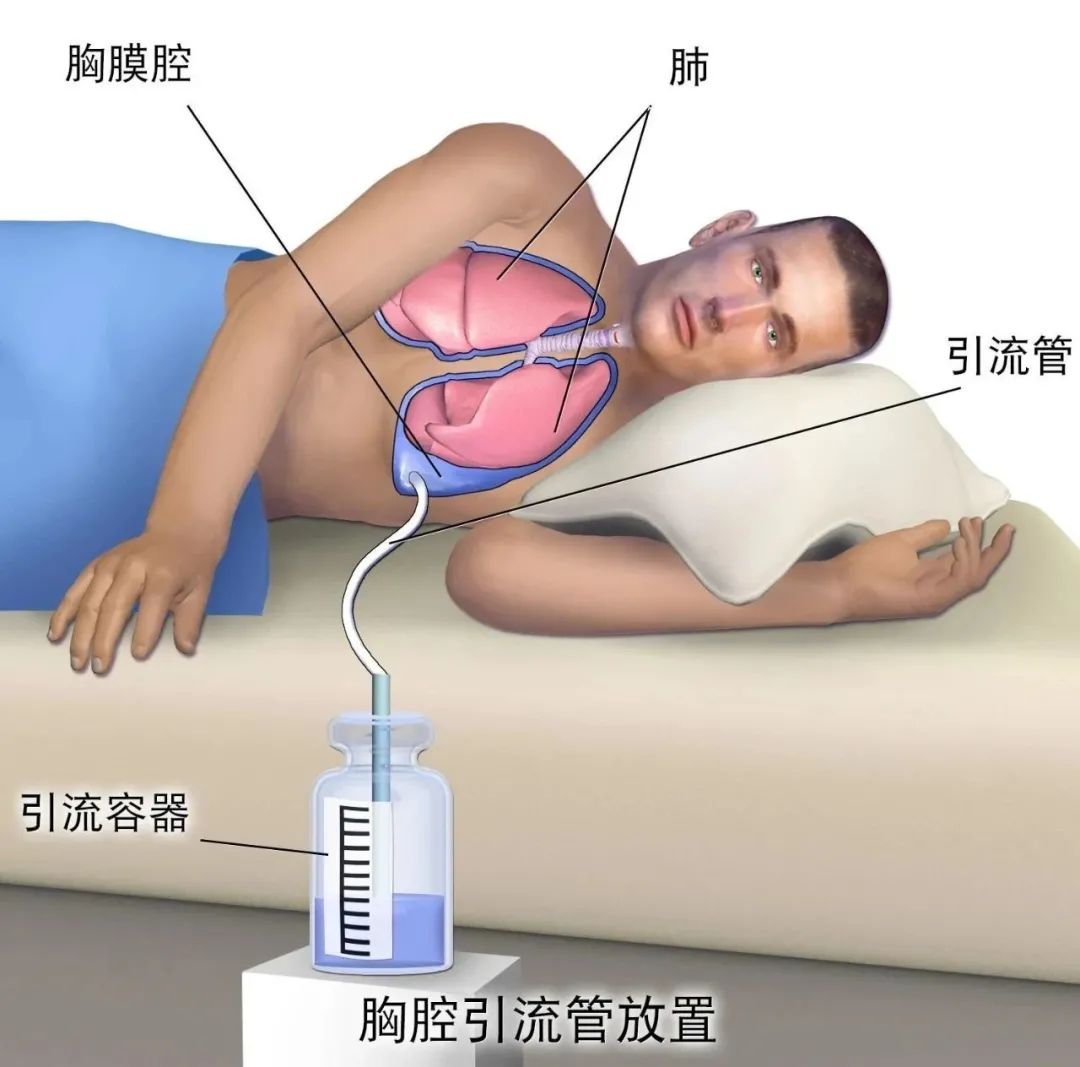
肺癌是全球发病率第二,死亡率第一的恶性肿瘤,随着近二十年肿瘤分子病理学和靶向治疗理念的飞速提升,肺癌从“全身性、系统性”疾病,逐渐演变成了以分子特征区分的一组疾病,其诊疗跨入精准时代,患者的生存期和生存质量得到显著提高。 肿瘤精准治疗的前提,是精准检测,基因检测作为晚期非小细胞肺癌肺癌诊疗的重要环节,逐渐被广大患友熟知,但同时也伴随着很多疑惑,比如,基因检测非做不可吗?检测项目众多挑花了眼,该怎么合理选择呢?基因检测做一次就够吗?组织样本检测好还是液体样本检测好?.....别急,听我们细细道来。 为什么要做基因检测? 指导靶向治疗的基因检测因此被赋予了重要意义,基因检测已经成为肺癌患者接受靶向治疗的基本前提。基因检测的必要性主要出于以下几点: 第一,一旦检出驱动基因阳性,意味着患者可以“量体裁衣,精准打靶”,从靶向治疗中获益; 第二,基因检测结果更好的帮助预测预后和复发风险,例如伴随TP53/ target=_blank class=infotextkey>P53突变可能意味着预后较差; 第三,可增加入组靶向药物临床研究的机会,最大化治疗希望。 举一个例子,EGFR 外显子20插入突变,作为EGFR罕见突变中最常见的亚型,长久以来药物研发之路坎坷,但随着莫博赛替尼等创新药物在我国获批上市,一旦检测出该类突变,患者在莫博赛替尼的治疗下,生存可能得到极大改善。 肺癌基因检测需要做哪些项目? NCCN非小细胞肺癌临床实践指南中对于“分子诊断与靶向治疗原则”(NSCL-G)明确指出肺癌基因检测时一定要包含这8种基因靶点:EGFR、ALK、ROS1、RET、BRAFV600和MET14外显子跳跃突变、KRAS、NTRK(1类推荐证据),扩展基因为包括MET扩增或过表达、HER-2等(2A类推荐证据)。 检测方法应选择经国家官方批准的试剂和平台设备,目前临床中常见的肺癌基因检测技术大致分为:二代测序技术(NGS)、实时聚合酶链反应(PCR)、免疫组织化学法(IHC)和荧光原位杂交技术(FISH)等,其中NGS或RT-PCR法可同时检测全部必检基因和扩展基因,应用相对广泛,NGS由于涵盖广泛的基因位点,还可提供额外的基因变异信息,更有助于临床判断预后和复发等。 针对不同的基因突变使用不同的靶向药物治疗。所以,对于肺癌患者,特别是非小细胞肺癌,首选做包含必选基因的检测套餐,费用应该在3000-12000左右。如果费用受限,最好首选做EGFR基因检测,这个在国内是最常见的突变基因。目前,国内上市的大部分肺癌靶向药物已经进入医保,大大减轻患者经济负担。 晚期非小细胞肺癌耐药后还需要做基因检测吗? 肿瘤存在异质性,可以不断进化和演变。如果疾病进展,就意味可能出现了新的耐药基因,此时既往的基因检测结果无法再指导新的临床治疗方案,需要再做一次检测,根据检测结果是否需要调整治疗方案。 对于EGFR-TKI耐药患者,建议二次活组织检查进行继发耐药基因检测:①EGFR T790M检测;对于无法获取组织的患者,可用ctDNA行EGFR T790M检测(2A类推荐证据)。当ctDNA阴性时,仍应建议患者行组织检测以明确EGFR T790M突变状态。②MET扩增检测(2B类推荐证据)。 原发肿瘤和转移病灶均适于靶向驱动基因检测(1类推荐证据)。 耐药后检测对后续治疗具有重要的指导意义!如果后续检测出相关的耐药靶点突变,可根据临床指南进行相应的靶向药物处理,如果未检测到,也能选择免疫、化疗或联合治疗等多种方式,对于部分国内还尚未获批药物的耐药位点突变,还可以尝试报名参与药物临床研究。 哪种标本做基因检测更好呢? 做肿瘤基因检测,检测的是肿瘤细胞的基因突变,因此需要获取肿瘤细胞。常见送检标本类型有这三种。 1.肿瘤组织标本:主要包括手术、纤维支气管镜下活检、CT引导下肺穿刺、胸腔镜、淋巴结穿刺活检等方法获取的标本。这是最优样本,适合做过手术或确诊时做过活检取样的患者。 2.穿刺活检样本:通常是在局部麻醉下,用很细的针刺入疑似肿瘤,来获取少量细胞用于分析。创伤很小,可避免不必要的手术。 3.液体活检样本:主要是指对血液、胸腹水或脑脊液进行检测。当遇到患者无法取得足够组织,或者组织样本年代久远,可以考虑用血液等液体活检样本进行代替。 对于基因检测来说,肿瘤组织是最好的样本,但有时候如果肿瘤部位在组织中占比非常少,难以取到,那就要在病理医生的指导下做肿瘤细胞富集,再做基因检测,尽可能保证取样精确。 精准诊疗,检测先行,已经成为非小细胞肺癌的诊疗共识。多基因联合检测是目前肺癌诊疗的趋势,更准确的检测结果有助于疾病诊断,进一步指导后续量身定做治疗方案,最大程度的提高患者的生存期和生存质量,并减轻患者的负担。